Группа Марии Рубель работает над исследованием поведения ДНК-наносенсоров при детекции сложных фрагментов: фрагментов с прочной вторичной укладкой, повторяющимися участками, высоко вариабельными или гуанин-цитозин богатыми участками. Также группа Марии собирает и систематизирует ранее накопленные материалы, формируя базу данных, для обучения искусственного интеллекта, который будет в будущем будет заниматься подбором и разработкой ДНК-наносенсоров. Эта работа позволяет лучше понимать функционирование ДНК-наносенсоров и готовит их для перехода в диагностическую практику.
Группа Муханнада Атейи занимается разработкой высокочувствительных ДНК-наноконструкций для безамплификационной детекции нуклеиновых кислот. Будучи наиболее чувствительным зондом среди бесферментных подходов, бинарные дезоксирибозимы (BiDz) по-прежнему недостаточно чувствительны для обнаружения большинства биологических ДНК или РНК-аналитов без амплификации. Наши усилия по увеличению предела обнаружения (LOD) BiDz-зондов привели к созданию конструкции, позволяющей увеличить скорость диффузии флуоресцирующего субстрата (F-sub) к ядру активированного BiDz-зонда, так называемой ДНК-наномашине (рисунок 1). Мы стремимся к дальнейшему совершенствованию этой конструкции за счет увеличения количества расщепляющих элементов, увеличения количества рук, связывающих аналит, и дальнейшего увеличения скорости диффузии F-sub. В результате реализации этих модификаций мы полагаем, что разработанная ДНК наноконструкция может повысить эффективность детекции до аттомолярных концентраций, что соответствует концентрации РНК в клетках. Разработанная ДНК-наноконструкция может быть использована для создания диагностических устройств, которые можно использовать для point-of-care диагностики и в условиях, когда стадия амплификации невозможна. Кроме того, этот подход может стать основой для разработки автоматического устройства для диагностики возбудителей и других прикладных целей.
Еще одно направление — разработка флуоресцентных гибридизационных зондов для высокоселективного обнаружения двухцепочечной ДНК (дцДНК). Специфическое связывание дцДНК с помощью гибридизационного зонда в физиологических условиях может быть использовано для нокдауна генов, картирования хромосом в живых клетках, обнаружения важных диагностических целей и, в конечном итоге, может привести к новым стратегиям терапевтического вмешательства против генетических заболеваний. Мы стремимся разработать такие конструкции с использованием модификаций ДНКзимов и закрытых (loked) нуклеиновых кислот (LNA). Все конструкции проходят две стадии разработки: оптимизация количества и положения модификаций LNA относительно каталитического ядра и тестирование конструкций в близких к физиологическим условиях и при различных температурах. Достигнув нашей цели, мы надеемся продвинуть будущее гибридизационных зондов за счет их превращения в ДНК-машины как более сложный сенсорный и специализированный инструмент.
Группа Дарьи Горбенко занимается оптимизацией некоторых видов ДНК - проб, преимущественно, типов 4-way-junction(4WJ) и мультикомпонентных пероксидазных машин. Основной задачей группы является интеграция существующих и показавших себя эффективными in vitro сенсоров в компактные системы детекции. Основные направления на сегодняшний день:
◦ внедрение хемилюминесентных ДНК-сенсоров в микрофлюидный датчик;
◦ иммобилизация и хранение ДНК- сенсоров на твердых подложках (нитроцеллюлозные мембраны, модифицированные стекла);
◦ биоконъюгация ДНК-сенсоров на наночастицах для последующей детекции в системах количественного подсчета сигнала / визуальной агрегации наночастиц как качественного показателя обнаружения искомого анализируемого агента.
Группа Татьяны Земеровой занимается разаботка тест-системы по генотипированию штаммов Mycobacterium tuberculosis. Основная проблема в лечении туберкулеза - устойчивость к антибиотикам разных штаммов бактерии, поэтому разработка системы, позволяющей быстро и без крупных затрат генотипировать штаммы может значительно повысить эффективность лечения. Штаммы отличаются друг от друга наличием/отсутствием мутаций – однонуклеотидных полиморфизмов (SNP), и на детекцию наличия/отсутствия SNP и направлена разработка. Объектом исследования является токсин-антитоксин система, функционирующая в бактерии с целью избегания действия антибиотиков. Разрабатываемая тест-система по генотипированию состоит из чувствительных к SNP ДНК-машин, и нашей целью является непосредственная детекция двуцепочечного целевого учатска. Также нашей целью является разработка мультиплексной системы, позволяющей детектировать до трех образцов в одном реакционном растворе, что еще больше сократит время и сложность анализа.
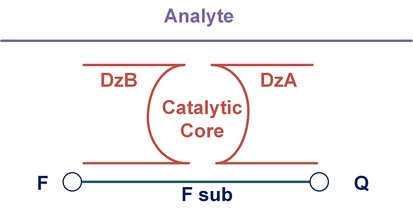
Рис. 1. Дизайн бинарного дезоксирибозима.
Внешний консультант лаборатории - Дмитрий Михайлович Колпащиков.
